Đốt cháy hoàn toàn 0,125mol hidrocacbon A thu được 25,7g CO2 và 11,25g H2O.
a/ Tìm CTĐGN, CTPT của A biết A có thể làm mất màu dd brom.
b/ Tính khối lượng dd brom 45% đủ để phản ứng với A
Đốt cháy hoàn toàn 1 hidrocacbon A sau phản ứng thu được 9,408 lít CO2 (đktc) và 7,56 gam H2O
a) Xác đinh CTPT của A. Biết tỉ khối của A so với khí He là 7
b) Chất A có làm nhạt màu dd Brom (dư) không? Tính khối lượng sản phẩm (nếu có)?
c) Dẫn toàn bộ lượng sản phẩm cháy thu được đi qua bình 1 đựng 90 gam đ H2SO4 96% và qua bình 2 đựng dd nước vôi trong (dư). Tính lượng nồng độ C% của axit rong 1 bình và lượng kết tủa thu được ở bình 2 sau khi phản ứng kết thúc
d) Nếu có hỗn hợp gồm khí A và SO2. Làm thế nào để thu được khí SO2 tinh khiết?
Giúp mình với! Mình đang cần lời giải gấp!
Mình cảm ơn!
a, Ta có: \(n_{CO_2}=\dfrac{9,408}{22,4}=0,42\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{7,56}{18}=0,42\left(mol\right)\Rightarrow n_H=0,42.2=0,84\left(mol\right)\)
Gọi CTPT của A là CxHy.
⇒ x:y = 0,42:0,84 = 1:2
→ CTPT của A có dạng (CH2)n.
Mà: \(M_A=7.4=28\left(g/mol\right)\)
\(\Rightarrow n=\dfrac{28}{12+2.1}=2\)
Vậy: A là C2H4.
b, - A là anken → có làm nhạt màu dd Br2 dư.
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Ta có: mC2H4 = mC + mH = 0,42.12 + 0,84.1 = 1,68 (g)
\(\Rightarrow n_{C_2H_4}=\dfrac{1,68}{28}=0,06\left(mol\right)\)
Theo PT: \(n_{C_2H_4Br_2}=n_{C_2H_4}=0,06\left(mol\right)\)
\(\Rightarrow m_{C_2H_4Br_2}=0,06.188=11,28\left(g\right)\)
c, - Bình 1: Ta có: \(m_{H_2SO_4}=90.96\%=86,4\left(g\right)\)
\(\Rightarrow C\%_{H_2SO_4}=\dfrac{m_{H_2SO_4}}{m_{ddH_2SO_4}+m_{H_2O}}=\dfrac{86,4}{90+7,56}.100\%\approx88,56\%\)
- Bình 2: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
Có: \(n_{CaCO_3}=n_{CO_2}=0,42\left(mol\right)\)
\(\Rightarrow m_{\downarrow}=m_{CaCO_3}=0,42.100=42\left(g\right)\)
d, - Dẫn hh gồm C2H4 và SO2 qua bình đựng Ca(OH)2 dư.
PT: \(SO_2+Ca\left(OH\right)_2\rightarrow CaSO_{3\downarrow}+2H_2O\)
- Lọc kết tủa, đem pư với dd HCl dư, thu khí thoát ra ta được SO2.
PT: \(CaSO_3+2HCl\rightarrow CaCl_2+SO_2+H_2O\)
Đốt cháy hoàn toàn 5,6 gam một hợp chất hữu cơ A, sau phản ứng người ta thu được 8,96 lít CO2 và 7,2 gam H2O
a) Lập CTPT của A biết tỉ khối hơi của A so với khí oxi là 0,875
b)Viết công thức cấu tạo của A
c)A có làm mất màu dd Brom ko.vì sao?
a) \(n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
\(n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\)
Bảo toàn C: nC = 0,4 (mol)
Bảo toàn H: nH = 0,8 (mol)
Xét mC + mH = 0,4.12 + 0,8.1 = 5,6 (g)
=> A chứa C, H
Xét nC : nH = 0,4 : 0,8 = 1 : 2
=> CTPT: (CH2)n
Mà MA = 0,875.32 = 28 (g/mol)
=> n = 2
=> CTPT: C2H4
b) CTCT: \(CH_2=CH_2\)
c) A có làm mất màu dd Br2 do A có tác dụng với Br2
\(CH_2=CH_2+Br_2\rightarrow CH_2Br-CH_2Br\)
Bài 1: Một Hidrocacbon X là chất lỏng có tỉ khối hơi so với không khí là 3.17. Đốt cháy hoàn toàn X thu được CO2 có khối lượng bằng 4.28 lần khối lượng h2o. Ở nhiệt độ thường X không làm mất màu dd brom, khi đun nóng X làm mất màu dd KMno4. Tìm CTPT
Bài 2: Cho benzen tác dụng với lượng dư Hno3 đặc có xúc tác h2so4 đặc để điều chế nitrobenzen. Tính khối lượng của nitrobenzen thu dc khi dùng 1 tấn benzen vs hiệu suất 78%
Thực hiện phản ứng crakinh butan thu được một hỗn hợp X gồm các ankan và các anken. Cho toàn bộ hỗn hợp X vào dd brom dư thấy có khí thoát ra bằng 60% thể tích X và khối lượng dd brom tăng thêm 5,6 gam và có 25,6 gam brom đã tham gia phản ứng. Đốt cháy hoàn toàn khí bay ra thu được a mol CO2 và b mol H2O. Vậy a, b có giá trị là
A. a = 0,9 và b = 1,5
B. a = 0,56 và b = 0,8
C. a = 1,2 và b = 1,6
D. a = 1,2 và b = 2
Đáp án B
Khi crakinh butan ta có các quá trình sau:
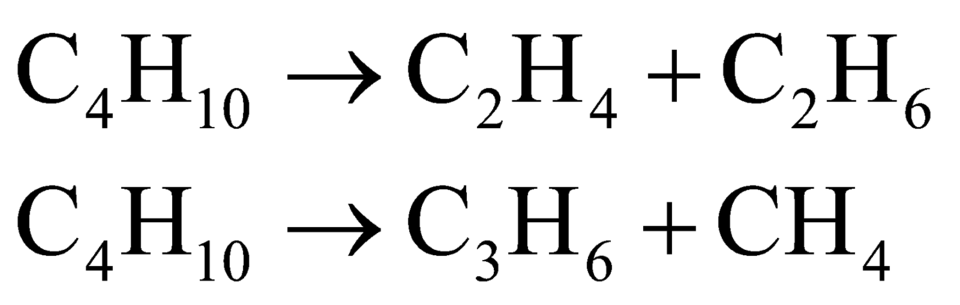
Nhìn vào các phản ứng dễ thấy nanken = nankan mói
Khi đi qua nước brom dư có 60% thể tích X thoát ra, suy ra có 40% X là anken đã phản ứng với brom
=> Có 40% ankan mới tạo thành và 20% butan dư.
Dễ tính được
nBr2=0,16 mol=> n anken=n Br2=0,16
=> nC4H10 du= n anken/2=0,08 mol
Tới đây đề bài đã cho khối lượng hỗn hợp anken, số mol hỗn hợp anken nên có thể tính được số mol mỗi anken trong hỗn hợp
Gọi số mol C3H6 và C2H4 lần lượt là x và y ta có hệ
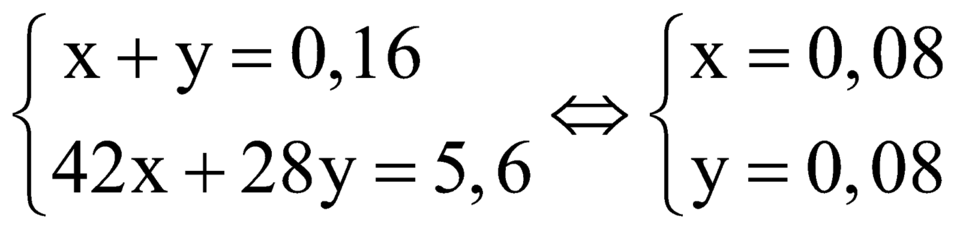 .
.
Khi đó khí bay ra gồm có

Đốt hỗn hợp này ta thu được
![]()
Bài 7: Một hydrocacbon A lỏng có dA/kk = 2,69
Đốt cháy A thu được CO2 và H2O theo tỷ lệ khối lượng 4,9: 1. Tìm:
a. CTPT của A.
b. Cho A tác dụng với Brom theo tỉ lệ mol 1:1 có Fe thu được B và khí C. Khi C hấp thụ hoàn toàn trong 2 lít dd NaOH 0,5 M. Để trung hoà NaOH dư cần 0,5 lít dd HCl 1M. Tính khối lượng của A tham gia phản ứng và khối lượng sản phẩm B tạo thành
MA=2,69.29=78g/mol
A là HC dạng lỏng nên A có số C>=5
Gọi CT A là CxHy
mCO2:mH2O=44x/9y=4,9/1
=>44x=44y
=>x=y
CTĐGN của A làCxHx M=14x
mà M=78 số C lớn hơn hoặc bằng 5 nhg loại 5 vì số H phải chẵn nên A là C6H6 benzen
C6H6+Br2 xt Fe,đun nóng=>C6H5Br + HBr
HBr+NaOH=>NaBr+H2O
nNaOH dư=nHCl=0,5 mol
nNaOH bđ=1 mol
=>nNaOH pứ=0,5 mol=nHBr
=>mA=0,5.78=39 gam
mB=0,5.157=78,5 gam
Đốt cháy hoàn toàn a(g) hỗn hợp 2 olefin đồng đẳng kế cận, sản phẩm cháy vào nước vôi trong dư thu được 55g kết tủa. Mặt khác a(g) vào dd brom làm mất màu 250ml brom 1M.
a/ Tìm CTPT 2 olefin. tính a.
b. Tính m mỗi olefin trong hỗn hợp và thể tích O2 (đktc).
m.n giúp mk vs ạ. cảm ơn nhiều
a. Gọi công thức chung là CnH2n (n không nhỏ hơn 2)
\(n_{kt}=0,55mol=n_{CO_2}=n_{H_2O}\)
\(n_{anken\left(olefin\right)}=n_{Br_2}=0,25mol\)
=> n = 0,55 : 0,25 = 2,2
=> 2 olefin đó là C2H4 và C3H6.
a = 0,25(12.2,2 + 2.2,2) = 7,7 g
b. Gọi số mol C2H4, C3H6 trong hh lần lượt là u, v mol
n(hỗn hợp) = u + v = 0,25
m(hỗn hợp) = 28u + 42v = 7,7
=> u = 0,2; v = 0,05
=> %mC2H4 = 72,73%
=> %mC3H6 = 27,27%
anken nCo2 = nH20
- Ca(oh)2 dư => 55g kết tủa = CaCO3 => nCO2 = nH20 = 0.55 mol
=>> a = 0.55*(12+2) = ?
mol hỗn hợp = 0.25 mol => khối lượng trung bình = a / 0.25
=>> hỗn hợp
Đốt cháy hoàn toàn a(g) hỗn hợp 2 olefin đồng đẳng kế cận, sản phẩm cháy vào nước vôi trong dư thu được 55g kết tủa. Mặt khác a(g) vào dd brom làm mất màu 250ml brom 1M.
a/ Timf CTPT 2 olefin. tính a.
b. Tính m mỗi olefin trong hỗn hợp và thể tích O2 (đktc).
m.n giúp vs ạ
a, Ta có: \(n_{CO_2}=n_{CaCO_3}=\dfrac{55}{100}=0,55\left(mol\right)\)
\(n_{hh}=n_{Br_2}=0,25.1=0,25\left(mol\right)\)
Gọi CTPT chung của 2 olefin là \(C_{\overline{n}}H_{2\overline{n}}\)
\(\Rightarrow\overline{n}=\dfrac{n_{CO_2}}{n_{hh}}=2,2\)
Mà: 2 olefin đồng đẳng kế tiếp.
→ C2H4 và C3H6.
\(\Rightarrow\left\{{}\begin{matrix}n_{C_2H_4}+n_{C_3H_6}=0,25\\2n_{C_2H_4}+3n_{C_3H_6}=0,55\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_{C_2H_4}=0,2\left(mol\right)\\n_{C_3H_6}=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow a=m_{C_2H_4}+m_{C_3H_6}=0,2.28+0,05.42=7,7\left(g\right)\)
b, mC2H4 = 0,2.28 = 5,6 (g)
mC3H6 = 0,05.42 = 2,1 (g)
Có: nH2O = nCO2 = 0,55 (mol)
BTNT O, có: \(2n_{O_2}=2n_{CO_2}+n_{H_2O}\Rightarrow n_{O_2}=0,825\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,825.22,4=18,48\left(l\right)\)
Đốt cháy 3,2g chất hữu cơ A thu được 8,8g CO2 và 7,2g H2O.
a. Hợp chất A gồm những nguyên tố gì?
b. Biết PTK A nhỏ hơn 30, cho biết CTPT và CTCT của A. Viết PTHH xảy ra.
c. Hợp chất hữu cơ A có làm mất màu dd brom không? Vì sao?
a) \(n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)\)
=> nC = 0,2 (mol)
\(n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\)
=> nH = 0,8 (mol)
Xét mC + mH = 0,2.12 + 0,8.1 = 3,2 (g)
=> A chứa C, H
b) Xét nC : nH = 0,2 : 0,8 = 1 : 4
=> CTPT: (CH4)n
Mà PTKA < 30 g/mol
=> n = 1 thỏa mãn
=> CTPT: CH4
CTCT:
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
c) A không làm mất màu dd Br2 do trong phân tử chỉ chứa liên kết đơn
bạn ơi sao xét m+m thì bt có chứa j vậy